Quand on parle de maladies vectorielles, on imagine souvent un duo de type moustique–humain avec, au milieu, un parasite ou un virus qui passe de l’un à l’autre au moment de la piqûre. En réalité, c’est une interaction à trois termes, avec des intérêts qui ne coïncident pas toujours : le vecteur arthropode (moustique, tique, mouche tsé‑tsé, phlébotome…), l’hôte vertébré et le microorganisme transmis.
Le vecteur a besoin de sang pour se reproduire, mais doit limiter les risques (prédation, défenses de l’hôte). L’hôte cherche à éviter les piqûres et les agents infectieux qu’elles transportent. Le microorganisme, lui, dépend entièrement du vecteur pour passer d’un hôte à l’autre et assurer sa survie évolutive. On peut donc se poser la question de savoir dans quelle mesure ces agents vectoriels peuvent‑ils manipuler à la fois l’hôte et le vecteur pour optimiser leur transmission ?
La peau, son microbiome et l’odeur qui attire les vecteurs
Les vecteurs ne se jettent pas au hasard sur un hôte. La localisation d’une source de sang, d’un hôte, repose sur différents mécanismes : des signaux de longue distance comme le CO₂ et certains composés volatils, puis des indices plus fins quand ils se rapprochent, avec un rôle central des odeurs corporelles à courte distance.
Ces odeurs proviennent en grande partie des microorganismes qui colonisent la peau. Bactéries et champignons dégradent la sueur, le sébum et les cellules mortes en une série de molécules volatiles. Le mélange final, notre “odeur”, dépend donc étroitement de la composition du microbiome cutané, qui varie énormément d’un individu à l’autre.
Des travaux cités dans la revue montrent, par exemple, que des moustiques anthropophiles sont plus attirés par des humains dont le microbiote cutané présente une densité bactérienne élevée et une diversité plus faible. Certaines espèces, notamment des Staphylococcus, produisent des bouquets odorants particulièrement attractifs, et cette association se retrouve dans plusieurs systèmes, des moustiques paludéens aux punaises en passant par des moucherons piqueurs.
En d’autres termes, notre flore de peau fonctionne comme une carte de visite chimique pour les vecteurs. Certains profils microbiens rendent littéralement un individu facile à trouver pour un moustique, alors que d’autres le rendent relativement discret. Cette hétérogénéité expliquerait déjà une partie de la variabilité inter‑individuelle dans le risque de piqûre. Mais l’article va plus loin : il montre que des pathogènes eux‑mêmes peuvent intervenir sur ce levier.
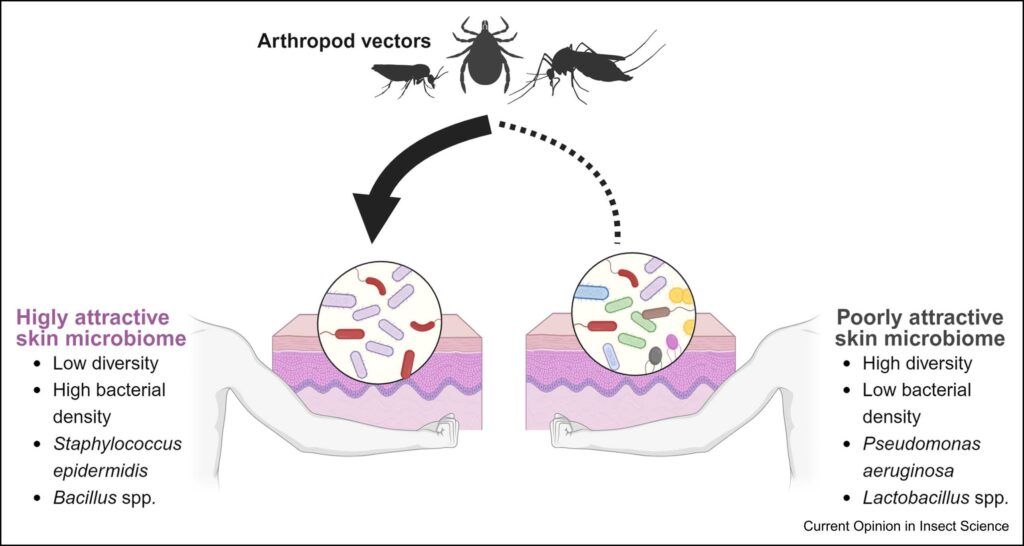
Les micro‑organismes cutanés influencent la préférence d’hôte des vecteurs arthropodes non infectés. La composition du microbiome de la peau et la présence d’espèces ou de souches bactériennes spécifiques modulent la préférence des vecteurs arthropodes, en affectant l’attractivité des hôtes vertébrés non infectés.
Quand l’infection change l’odeur de l’hôte
Un résultat général qui ressort de la littérature est le suivant : dans de nombreux systèmes, les vertébrés infectés par des agents vectoriels deviennent plus attractifs pour les vecteurs que leurs congénères non infectés. Cela a été montré avec des parasites du genre Leishmania, avec Plasmodium falciparum (paludisme) ou encore avec des infections à Borrelia chez des rongeurs. Dans des tests de choix, phlébotomes, moustiques ou tiques préfèrent systématiquement les hôtes infectés.
Dans plusieurs cas, cette attractivité accrue est associée à des modifications de l’odeur corporelle, elles‑mêmes liées à des changements du microbiome cutané. Des souris infectées par Leishmania présentent une dysbiose de la peau : leur flore se rapproche de celle observée chez des individus naturellement très attractifs. L’odeur qui en résulte attire davantage les phlébotomes vecteurs, ce qui augmente mécaniquement la probabilité de transmission.
Le cas des arbovirus comme la dengue ou Zika est particulièrement éclairant. Une étude discutée dans l’article suit toute la chaîne causale : infection par le virus, modulation de l’immunité cutanée, altération ciblée du microbiome, changement de l’odeur, augmentation de l’attraction des moustiques. Concrètement, l’infection enrichit des bactéries capables de produire l’acétophénone, un composé volatil très attractif pour les moustiques. Ce basculement microbien résulte d’une down‑régulation d’un peptide antimicrobien de l’hôte : en réduisant l’expression de ce peptide, le virus relâche la pression sur certaines bactéries de la peau, qui prolifèrent et émettent davantage de molécule attractive.
Ce type de résultat est important : on ne se contente plus de constater qu’un hôte infecté sent différemment, mais on commence à identifier des maillons précis. Un produit viral agit sur l’immunité locale (peptides antimicrobiens, cytokines), ce qui modifie la composition microbienne, qui à son tour modifie les signaux olfactifs perçus par le vecteur. Dans le modèle dengue/Zika, restaurer le peptide antimicrobien, par exemple via une supplémentation en vitamine A, atténue cette dérive du microbiome.
L’arthropode infecté, un vecteur au comportement modifié
Du côté du vecteur, le microorganisme doit franchir plusieurs barrières : intestin moyen, hémolymphe, glandes salivaires, parfois tissus nerveux. Ce trajet prend du temps et interagit avec l’immunité du vecteur. Il n’est donc pas surprenant que l’infection s’accompagne fréquemment de modifications de la physiologie et du comportement.
L’article passe en revue divers exemples. Des tiques infectées par Borrelia burgdorferi ou par des virus d’encéphalite montrent une activité et une mobilité accrues, ainsi qu’une agressivité plus forte dans leur quête d’hôte. Ces changements augmentent la probabilité de contact avec un vertébré, donc la transmission potentielle du pathogène. Chez des moustiques porteurs des stades transmissibles de Plasmodium, on observe des décalages des rythmes d’activité et des modifications de l’expression de gènes chémosensoriels : leurs pics de quête d’hôte coïncident mieux avec les périodes où les humains sont accessibles, ce qui est cohérent avec l’intérêt du parasite.
La sensibilité aux odeurs d’hôte peut elle aussi être modifiée. Plusieurs études montrent une réponse renforcée de vecteurs infectés à certains signaux olfactifs, même si ce n’est pas universel et que certains systèmes ne retrouvent pas cet effet. L’ensemble suggère toutefois que de nombreux pathogènes n’affectent pas seulement la santé du vecteur, mais aussi la façon dont il perçoit et utilise les indices chimiques de son environnement.
Un point intéressant, sur le plan évolutif, est que ces altérations comportementales ne sont pas uniformes au cours de l’infection. Elles tendent à être plus marquées lorsque le microorganisme est effectivement transmissible, par exemple lorsqu’il a atteint les glandes salivaires chez les moustiques. Cela plaide en faveur d’un ajustement au stade infectieux plutôt que d’un simple effet uniforme.
La prise de sang : goulot d’étranglement et point de contrôle
La rencontre entre un vecteur et un hôte ne suffit pas à garantir la transmission. Il faut encore que la piqûre aboutisse à un repas sanguin, avec injection de salive et temps de contact suffisant. La phase de prise de sang apparaît donc comme un goulot d’étranglement clé, et de fait, un grand nombre de manipulations décrites concernent précisément cette étape.
Chez la mouche tsé‑tsé infectée par Trypanosoma brucei, par exemple, la composition de la salive change de manière à rendre la prise de sang plus difficile. Le repas devient plus long, la mouche multiplie les essais, ce qui augmente les occasions de transfert du parasite vers un hôte vertébré. Ce qui est défavorable à l’insecte peut ainsi être très favorable pour le trypanosome.
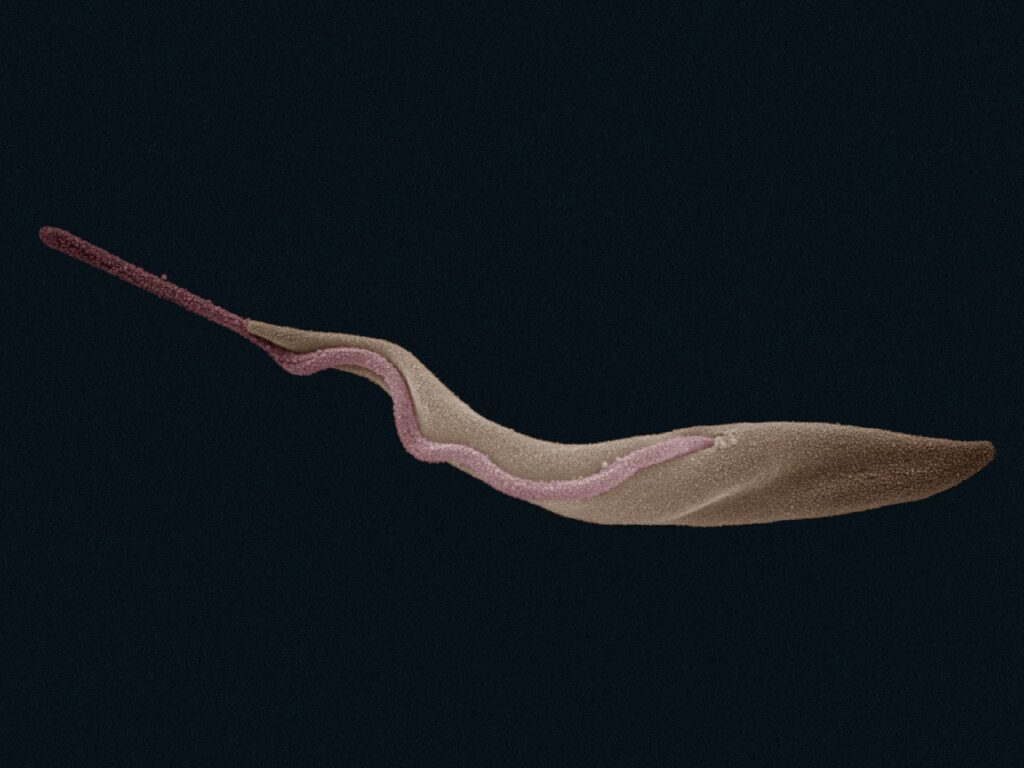
Image MEB en fausses couleurs d’une forme de Trypanosoma brucei, stade présent dans l’intestin de la mouche tsé‑tsé. Le corps cellulaire apparaît en brun et le flagelle, essentiel à la motilité et aux interactions avec l’hôte vecteur, est mis en évidence par une coloration différente. (@By Zephyris – Own work, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=10769382)
Des enregistrements vidéo rapprochés réalisés chez des moustiques infectés par le virus de la dengue montrent également des modifications fines du comportement de piqûre. Par rapport à des témoins non infectés, ces moustiques effectuent davantage de tentatives de repas, parfois sans obtenir de volume de sang significatif. Ces tentatives de repas suffisent néanmoins à déposer le virus dans la peau de plusieurs hôtes successifs. On se retrouve donc avec des repas moins efficaces du point de vue de l’insecte, mais potentiellement beaucoup plus rentables pour le virus, qui peut être transmis à plusieurs individus en un laps de temps limité.
Au‑delà de ce qu’on voit à l’œil nu, l’article insiste sur l’importance de paramètres cachés : la durée de salivation, le délai avant de trouver un vaisseau sanguin, le temps d’ingestion, etc. Ces variables influencent directement la probabilité de transmission, mais nécessitent des outils complexes pour être étudiées. Des travaux en entomologie végétale montrent déjà que des virus de plantes modifient ces paramètres chez leurs vecteurs pour optimiser leur diffusion.
Manipulation ciblée ou simple effet collatéral ?
Faut‑il pour autant considérer toutes ces modifications comme des manipulations au sens strict ? Les auteurs de la revue invitent à la prudence. Une infection entraîne forcément des changements physiologiques : inflammation, stress oxydatif, dérèglements métaboliques… Certains de ces effets peuvent, par hasard, augmenter la transmission sans avoir été façonnés spécifiquement par la sélection naturelle.
Pour parler de véritable manipulation adaptative, deux critères sont proposés. D’abord, identifier des produits du pathogène (métabolites, protéines, effecteurs) qui ciblent explicitement des voies de l’hôte ou du vecteur (par exemple un peptide antimicrobien cutané, une cytokine, un neurotransmetteur). Ensuite, démontrer que l’effet de ces produits se traduit bien par une augmentation de la transmission.
Le cas du métabolite HMBPP produit par Plasmodium falciparum, qui augmente la libération de CO₂ et d’autres volatils attractifs par les globules rouges infectés, entre dans cette logique, même si toutes les conséquences sur les odeurs de peau et l’attraction des moustiques restent à préciser. De même, l’exemple des flavivirus modulant un peptide antimicrobien cutané pour enrichir certaines bactéries productrices d’acétophénone coche plusieurs cases de la définition.
On est donc face à un continuum : à une extrémité, des effets purement collatéraux de l’infection ; à l’autre, des manipulations fines, où l’on peut retracer la chaîne depuis une molécule produite par le pathogène jusqu’au comportement final de l’hôte ou du vecteur. Une partie du travail actuel consiste à positionner chaque système réel le long de ce gradient.
Exploiter cette écologie invisible pour la lutte antivectorielle
Comprendre comment des microorganismes modulent les signaux d’attraction et le comportement des vecteurs ne relève pas uniquement de la curiosité théorique. Cela ouvre de nouvelles pistes pour la lutte antivectorielle, en complément des moustiquaires, insecticides et vaccins.
L’une des idées discutées dans l’article est d’utiliser les caractéristiques des microbiomes cutanés peu attractifs comme modèles à imiter. Si certains profils bactériens rendent objectivement l’hôte moins appétissant pour les moustiques, on peut imaginer des approches de type pré‑ ou probiotique cutané pour orienter la flore de la peau dans ce sens, au moins chez des populations très exposées.
Autre levier : les pièges olfactifs. Des dispositifs combinant CO₂ et mélanges de composés volatils humains ont déjà montré une réduction d’incidence du paludisme dans certains essais. Les enrichir avec des signaux dérivés de bactéries de peau caractéristiques des “super attractifs” pourrait encore augmenter leur efficacité et leur capacité à détourner les vecteurs des habitations.

Piège à moustiques utilisant des indices de localisation similaires à ceux exploités par les vecteurs en quête d’hôte : émission contrôlée de CO₂, diffusion de composés odorants et aspiration mécanique vers un filet de capture. (Photo @Biogents)
Enfin, des outils inspirés des bactériophages, comme des endolysines ciblant spécifiquement certaines espèces cutanées particulièrement attractives, sont évoqués comme une perspective à plus long terme. L’idée générale est de ne plus considérer la peau comme un simple support passif, mais comme un écosystème qu’on peut moduler pour rendre la rencontre vecteur–hôte moins probable ou moins productive pour le pathogène.
Cette vision des maladies vectorielles, centrée sur les interactions microorganismes–vecteurs–microbiomes, complexifie le tableau, mais elle ouvre aussi des angles de prévention auxquels on ne pensait pas il y a vingt ans.
Pour une exploration plus approfondie, je ne peux que vous inviter à consulter l’article:
Article Source: Bourne ME, Lucas‑Barbosa D, Verhulst NO. Host location by arthropod vectors: are microorganisms in control? Curr Opin Insect Sci. 2024;65:101239. doi:10.1016/j.cois.2024.101239.




Commentaires récents